Tot sobre l'osmi

Osmi - un metall rar, pertany al grup del platí. Va ser descobert a Anglaterra com a resultat d'experiments sobre la reacció del platí. El nom d'osmi es dóna en grec i en la traducció significa "olor". Com és aquest metall noble? Quines són les seves característiques i quin és el seu ús?

Història
El descobriment d'aquest element va ocórrer per accident l'any 1803 pels químics anglesos Smithson Tennant i William H. Wollastan. Com a resultat dels experiments sobre la reacció del platí amb una barreja d'àcids (sulfúric i nítric), el precipitat resultant va desenvolupar una aroma desagradable, que recordava la pudor del clor i el rave podrit. Experiments similars van ser realitzats per Colle-Descoti, Antoine de Fourcoy i Vauquelin a França. Com a resultat de la seva investigació, també van trobar una substància desconeguda en el sediment insoluble del platí.



La substància desconeguda aleshores va rebre el nom de pollet, però els experiments dels britànics van demostrar que es tracta de dues substàncies semblants: iridi i osmi.
El descobriment d'aquests elements químics es va presentar a la Royal Society de Londres per una comunicació escrita de Tennant datada el 21 de juny de 1804. A la taula periòdica dels elements químics de Mendeleiev, el metall es troba sota el nombre ordinal 76. El metall no es presenta en forma pura per pepita, per tant la seva fórmula química es presenta en forma dissolta.


L'element s'extreu de matèries primeres secundàries com a conseqüència de la seva separació dels minerals d'iridi, platí, platí-pal·ladi o de coure i níquel. La producció anual de tot l'element al món no supera la mida d'1 tona.


Lloc de naixement
Els jaciments més grans del món són dignes de destacar zones com Muntanyes Urals i Sibèria a Rússia, estat del nord Alaska i l'estat occidental Califòrnia a Amèrica, Canadà a Amèrica del Nord, Colòmbia a Amèrica del Sud i alguns països sud-africans, Austràlia, Illa Tasmània... Actualment, es considera un important dipòsit d'osmi Bushwell Complex a Sud-àfrica, la major part de la substància s'extreu allà. Tenint en compte que els jaciments més grans del metall es troben a Sud-àfrica, els preus mundials d'aquest metall de terres rares són força elevats. Kazakhstan es considera l'únic gran exportador d'osmi-187 al món. Tot i que la Xina té reserves de mineral de platí, no té quantitats significatives d'osmi.


La substància s'emmagatzema en forma de pols i com que no es fon en forma de cristalls, no és possible posar-hi un segell per les seves propietats físiques. Per a la fabricació de lingots d'aquest metall, s'utilitza escalfament per feix d'electrons o arc a partir d'una pols; també s'utilitza l'escalfament en un gresol.


Propietats
L'osmi sembla un metall blavós platejat. És un dels elements més densos, la seva densitat és de 22600 quilograms per metre cúbic, però al mateix temps la substància és bastant fràgil, es trenca i s'esmicola fàcilment. Té una alta gravetat específica i és capaç de brillar fins i tot amb influències de temperatura força altes. A causa dels seus paràmetres i de la seva important temperatura de fusió, és difícil mecanitzar-lo. A la natura, existeix en forma de set isòtops, sis dels quals es consideren estables, aquests són osmi-184, osmi-187, osmi-188, osmi-189, osmi-190 i osmi-192. Al laboratori es van obtenir isòtops de metalls radioactius amb nombres en massa de 162 a 197 i també es van obtenir artificialment alguns isòmers nuclears.
L'osmi, per les seves característiques, afecta negativament a tots els organismes vius.

Gairebé tots els compostos amb aquest metall causen danys als òrgans interns, trastorns visuals i auditius. En cas d'intoxicació amb vapors d'osmi, es poden produir alteracions irreversibles en el cos i la mort. Els científics van realitzar experiments amb animals, els resultats dels quals van ser el ràpid desenvolupament de l'anèmia, la manca de funció pulmonar normal. Es va concloure que es tracta d'un edema de desenvolupament ràpid. El tetròxid d'osmi, que s'utilitza en medicina, és una substància molt corrosiva. Té l'olor més desagradable del món. En cas d'intoxicació, la pell pateix, canvia de color a verd o negre, sovint acompanyada d'úlceres i esquerdes, que trigaran molt a curar-se.

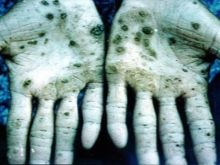

Els empleats de les instal·lacions de producció corren el risc més alt; segons totes les normes de seguretat, només treballen amb respiradors i roba especial. Tots els envasos que contenen òxid d'osmi estan tancats i emmagatzemats d'acord amb les normes. Per obtenir els minerals de la nevyanskita, el platí es converteix en solució mitjançant aqua regia. Aleshores, el precipitat resultant s'exposa al zinc en una quantitat de 8 vegades; aquest aliatge es converteix amb relativa facilitat en un estat en pols, que després es fusiona amb peròxid de bari. La següent etapa és el processament de la massa resultant amb aigua regia, destil·lació a través de l'aparell de separació del tetròxid d'osmi.

En actuar sobre la substància amb una solució alcalina s'obté sal. La solució salina es veu afectada hiposulfit, com a resultat de la qual, amb l'ajuda del clorur d'amoni, el metall precipita ja en forma de sal de Fremy. El precipitat es renta, es filtra i es calcina. El resultat de totes aquestes accions és l'osmi esponjós. Posteriorment, es neteja amb àcids, es redueix en un forn elèctric sota un corrent d'hidrogen i es refreda. Tan obtenir mostres d'osmi fins a un 99,9%.


Química
Les propietats d'aquest element, des del punt de vista de la química, són sorprenents. Els més bàsics d'ells són els següents.
- L'osmi no reacciona gens amb àlcalis i àcids. Forma osmates solubles en aigua en reacció amb les foses alcalines. La interacció amb una barreja d'àcids nítric i clorhídric dóna una reacció extremadament lenta.
- Molt tòxic, fins i tot en dosis microscòpiques. Especialment tòxic és l'òxid d'osmi, que s'allibera del platí.
- És impossible determinar el punt d'ebullició del metall, ja que és especialment refractari.
- El metall de la pols entra fàcilment en una reacció d'escalfament amb aquestes substàncies: oxigen pur, halògens, àcids sulfúric o nítric.
- En diversos compostos, rep nombres d'òxids de -2 a +8. Els més habituals són +2, +3, +4 i +8.
- Capaç de formar compostos de clúster.
- Els principals minerals estan relacionats amb solucions sòlides i estan representats per aliatges d'iridi amb osmi: són sysertskite i nevyanskite. A més, syserskite té un nom diferent: osmi iridiós, i nevyanskita - iridi osmós.

Física
Densitat l'osmi és d'aproximadament 22,61 grams per centímetre cúbic. Els cristalls tenen una bonica brillantor platejada, amb diferents matisos des del gris fins al blau. Als lingots apareix un color blau fosc, a la pols és violeta. Tot el metall té una brillantor platejada. La toxicitat de l'element impedeix el seu ús en la indústria de la joieria. Les principals propietats físiques són les següents.
- El punt de fusió d'aquest element és bastant alt, la fusió és possible a temperatures superiors als 3000 graus centígrads.
- El metall no té propietats magnètiques.
- Increïble fermesa. Els aliatges amb l'addició d'aquest metall adquireixen una major resistència al desgast, durabilitat, resistència a la corrosió i resistència a l'estrès mecànic.
- El punt d'ebullició és de 5012 ºC.
- La duresa de Mohs és 7.
- La duresa Vickers és de 3-4 GPa.

Aplicacions
A causa del cost important de l'element en si, aquest metall rarament s'utilitza en la producció industrial massiva. L'osmi s'utilitza principalment a la indústria química, on s'utilitza com a catalitzador. El tetròxid d'osmi s'utilitza en alguns medicaments. En anàlisis de laboratori, s'utilitza per tenyir teixits vius, assegura la preservació de l'estructura cel·lular.
A la indústria aeroespacial s'utilitza l'osmi en l'equip electrònic d'equips per a la tecnologia aeronàutica i de coets, així com en la fabricació armes nuclears. A causa de la manca de propietats magnètiques, el metall s'utilitza en la fabricació de rellotges de marca com Rolex. L'aliatge d'osmi amb platí s'utilitza quan creació d'implants quirúrgics Són marcapassos o vàlvules pulmonars.
A més, l'osmi s'utilitza en microscòpia i per crear instruments d'alta precisió.



Dades d'Interès
- Sota una pressió d'uns 770 GPa en osmi, els electrons interaccionen en orbitals interns, l'estructura de la substància roman inalterada.
- Osmi a les roques conté mig per cent de la massa total dels jaciments de mineral.
- A causa de l'alta densitat l'aspecte i el pes real del metall varia molt. Per tant, una ampolla de plàstic de 0,5 litres plena d'aquesta pols metàl·lica serà més pesada que una galleda de 10 litres plena d'aigua.
- Aquest metall es troba entre els cinc més costós.
- El cost d'una unça triple d'osmi és un secret comercial, a les fonts obertes podeu trobar un preu aproximat per 1 gram de substància.
- A causa de la refractarietat de l'osmi assenyalat en la història del llum elèctric. El científic K. Auer von Welsbach d'Alemanya va fer una proposta per substituir el filament de carboni d'una bombeta per un filament d'osmi. Les bombetes van resultar ser 3 vegades menys intensives en energia i la il·luminació ha millorat notablement. És cert que aviat va ser substituït pel tàntal més comú, que, al seu torn, va ser substituït pel tungstè.
- Una situació similar va passar amb el metall rar en la producció d'amoníac. El mètode de síntesi d'amoníac, que encara s'utilitza avui, desenvolupat l'any 1908 pel químic alemany Fritz Haber, és impossible sense l'ús de catalitzadors.Inicialment, els catalitzadors utilitzats en aquell moment mostraven les seves propietats només en presència de condicions de temperatura importants i no tenien una alta eficiència, per la qual cosa la recerca d'un substitut era molt rellevant. Científics del laboratori de l'Escola Tècnica Superior de Karlsruhe van fer una proposta per utilitzar osmi finament atomitzat com a element catalític. Els resultats de les proves van confirmar que aquesta idea val la pena, la temperatura catalítica ha baixat més de 100 ºC i l'alliberament d'amoníac ha augmentat significativament. És cert que en el futur es van negar a l'osmi, però va ajudar a resoldre un problema tan important.

L'osmi i altres metalls rars i únics juguen paper important en diferents sectors... Malgrat tota la seva toxicitat, salva vides i salut de persones.
Per obtenir més informació sobre l'osmi, mireu el següent vídeo.








